Alligator inleder kliniska studier med ATOR-1015: »Potentialen är enorm«
Idag meddelade bioteknikbolaget Alligator Bioscience att man erhållit nödvändiga myndighetstillstånd för att inleda en klinisk fas I-studie med sin huvudtillgång ATOR-1015, en helägd bispecifik immunonkologisk läkemedelskandidat. Bolaget påbörjar nu patientrekryteringen till studien som ska inkludera patienter med spridd cancer. BioStock kontaktade bolaget för en kommentar.
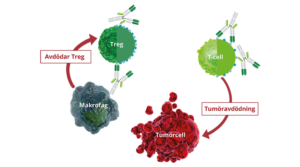
ATOR-1015 är en nästa generationens bispecifika immunstimulerande antikropp som binder till två olika målmolekyler samtidigt, CTLA-4 och OX40. Både CTLA-4 och OX40 överuttrycks på regulatoriska T-celler i tumörmiljön. ATOR-1015 minskar antalet regulatoriska T-celler och aktiverar effektor-T-celler vilket sammantaget ger en immunmedierad antitumöreffekt.
ATOR-1015 kan ge bättre effekt än två separata antikroppar som binder till CTLA-4 respektive OX40 eftersom den fysiskt binder molekylerna till varandra vilket främjar antitumöreffekten ytterligare.
Starka prekliniska resultat banar väg för kliniska studier
Kandidaten förväntas kunna användas för behandling av ett stort antal olika cancerformer och har s.k. First-In-Class-potential. Under det prekliniska programmet har ATOR-1015 testats mot urinblåse-, kolorektal-, pankreascancer och malignt melanom. I experimentella sjukdomsmodeller med ATOR-1015 erhöll de patienter som svarade på behandling livslångt skydd/immunitet mot angrepp från samma cancer.
Ska fastställa säkerhet och tolerabilitet
Med dessa starka prekliniska resultat i bagaget inleder nu alltså Alligator Bioscience en fas I-studie som ska inkludera upp till 53 patienter med spridd cancer på fem kliniker i Danmark och Sverige. Studien, som är den första i människa, är designad som en doseskaleringsstudie och syftar till att undersöka säkerheten och tolerabiliteten för ATOR-1015 samt till att fastställa en rekommenderad dos för efterföljande fas II-studier. Som bolaget tidigare kommunicerat har man utsett Theradex Oncology, ett globalt bolag med lång erfarenhet av klinisk utveckling av cancerläkemedel, som CRO (Contract Research Organization) för studien.
I ett pressmeddelande på tisdagmorgonen poängterar Alligator Bioscience vd Per Norlén, att starten av den kliniska fas I-studien med ATOR-1015 är en viktig milstolpe för Alligator, som enligt uppgift är först i världen med att ta fram en tumörlokaliserande CTLA-4-antikropp. Användningen av CTLA-4-blockerare har, trots bevisad effekt, hittills begränsats av allvarliga biverkningar. ATOR-1015 har dock enligt Per Norlén potentialen att lösa detta problem tack vare dess förmåga att selektivt aktivera immunsystemet i tumören men inte i resten av kroppen. Detta styrks enligt bolaget också av att ”de prekliniska resultaten ser väldigt lovande ut och stödjer konceptet fullt ut”.
BioStock kontaktade Per Norlén på Alligator för ytterligare kommentarer.
Studien kan omfatta upp till 53 patienter vid 5 kliniker i Sverige och Danmark. Hur snabbt förväntar ni er kunna rekrytera patienterna och när bedömer ni att studien kan vara färdig?
– Vi samarbetar i denna studie med flera av de kliniker vi arbetade med för ADC-1013 och har stort förtroende för deras förmåga att rekrytera patienter. Detta är en doseskaleringsstudie vilket innebär att det inte går att beräkna exakt slutdatum, men vanligtvis tar denna typ av studie 18-24 månader.
»Potentialen är enorm, Yervoy säljer idag för över 1 miljard dollar årligen bara inom hudcancer, och då kan endast 25 procent av dessa patienter använda läkemedlet p.g.a. allvarlig biverkansproblematik. Med ATOR-1015 har vi förhoppningar om att ha minst lika god effekt men utan allvarliga biverkningar, vilket ger möjlighet att behandla en långt större patientpopulation.« – Per Norlén, vd Alligator
Fas I-studien ska inkludera patienter med spridd cancer, inte friska frivilliga vilket annars ofta är fallet. Beror det på att ni, utöver att undersöka säkerhet och tolerabilitet, även kommer samla in tidig effektdata?
– När det gäller läkemedelskandidater som utvecklas mot cancer är det praxis att rekrytera patienter redan i de första studierna. Precis som du säger medger detta en möjlighet att även få information om läkemedelskandidatens effekt, även om man måste vara medveten om att studien i första hand genomförs för att studera säkerhet, och att eventuella effektsignaler därför alltid är att betrakta som osäkra i denna fas av utvecklingen. Målmolekylen CTLA-4 är sedan tidigare validerat effektiv (Yervoy) men förknippad med allvarlig biverkansproblematik. Det är här ATOR-1015 fungerar annorlunda, den är en tumörlokaliserande CTLA-4-antikropp som utvecklas för att ge kraftfull effekt i tumörmiljön utan att aktivera immunsystemet i resten av kroppen. Detta är ett helt nytt koncept för CTLA-4-antikroppar och stöds av prekliniska studier där ATOR-1015 uppvisat mycket god säkerhet/effektprofil.
Nobelprisvinnaren i medicin, Tasuku Honju nämnde i sitt segertal igår CTLA-4-hämmare som en av de två viktigaste målmolekylerna inom immunonkologi. Alligator är först i världen med en tumörlokaliserande CTLA-4-antikropp. Hur ser ni på värdepotentialen i projektet?
– Potentialen är enorm, Yervoy säljer idag för över 1 miljard dollar årligen bara inom hudcancer, och då kan endast 25 procent av dessa patienter använda läkemedlet p.g.a. allvarlig biverkansproblematik. Med ATOR-1015 har vi förhoppningar om att ha minst lika god effekt men utan allvarliga biverkningar, vilket ger möjlighet att behandla en långt större patientpopulation. Dessutom har Yervoy nu godkänts även för lungcancer vilket ökar patientpopulationen påtagligt. Potentialen är alltså ofantlig. Vår plan är att driva projektet själva genom fas II och på så sätt maximera värdet på ett framtida utlicensieringsavtal med en partner som kan genomföra de avslutande kliniska studierna och ta det till marknaden.
Innehållet i Biostocks nyheter och analyser är oberoende men Biostocks verksamhet är i viss mån finansierad av bolag i branschen. Detta inlägg avser ett bolag som BioStock erhållit finansiering från.