
Vd-intervju Alligator: "Det finns en stark drivkraft att utveckla nya, säkrare och mer effektiva immunterapier"
Årets nobelpris i fysiologi eller medicin sätter strålkastarljuset på det kanske mest lovande utvecklingsområdet för framtidens cancerbehandling, immunterapi. Forskarnas banbrytande upptäckter, att vårt eget immunsystem snillrikt kan användas för att bekämpa cancer, banade väg för ett av de mest tongivande svenska bolagen på den globala arenan, Alligator Bioscience. BioStock har träffat vd Per Norlén för att få veta mer om bolagets händelserika år, framtidsutsikterna och, inte minst, mångmiljardaffären med världens största hälsobolag.
»Dagens CTLA-4-läkemedel begränsas av svåra biverkningar, men ATOR-1144 har i likhet med ATOR-1015 möjlighet att undgå detta problem genom att den söker sig till tumörområdet« — Per Norlén, vd Alligator Bioscience

Per Norlén, vd Alligator Bioscience, ni är inne i en väldigt händelserik period. Den senaste nyheten är att ni kommer att få en utbetalning om drygt 30 Mkr från ert sydkoreanska partnerbolag AbClon Inc. efter att deras partner i sin tur valt att utöka sitt avtal med AbClon. Kan du förklara lite er om hur det hänger ihop?
– Vi har haft ett mångårigt samarbete med det Sydkoreanska bolaget AbClon Inc vilket har resulterat i framtagandet av flera olika terapeutiska antikroppar. Som en följd har Alligator en andel i eventuella intäkter från dessa projekt. 2016 utlicensierade AbClon de kinesiska rättigheterna till en av deras läkemedelskandidater, AC101, till Shanghai Henlius Biotech, Inc. Henlius har nu valt att utöka avtalet till att omfatta globala rättigheter vilket utlöser en betalning om cirka 90 Mkr till AbClon. Alligator har rätt till 35 procent av AbClons intäkter från Henlius.
Hur välkommet är detta kapitaltillskott?
– Det är självklart mycket välkommet, speciellt nu när vi går in i mer kostnadsintensiva faser med flera av våra läkemedelskandidater. Ytterligare ett projekt går in i klinisk utveckling i år och ytterligare ett eller till och med två projekt under nästa år.
Den 30 oktober stod det klart att ni inleder preklinisk utveckling av läkemedelskandidaten ATOR-1144. I pressmeddelandet säger ni er vara entusiastiska över denna nya immunterapeutiska läkemedelskandidat. Kan du berätta mer om beslutet att utvidga er pipeline ytterligare?
– Vi satsar mycket aktivt på att bygga och utveckla vår projektportfölj. Nu när övriga prekliniska projekt är på god väg fram mot klinisk fas är det naturligtvis glädjande att kunna fylla på med nya produkter från Discovery. Med den nyskapande ATOR-1144 levererar vi ännu en läkemedelskandidat som befinner sig i den absoluta framkanten inom immunonkologi.
»Alligator fokuserade så tidigt som 2008 helt på immunonkologi, d.v.s. flera år innan området var allmänt erkänt«
ATOR-1144 är en ”first-in-class” bispecifik tumör-lokaliserande antikropp vars verkningsmekanismen lämpar sig för behandling av såväl solida tumörer som blodcancer. På vilket sätt gör detta kandidaten unik?
– ATOR-1144 är en mycket intressant produkt som aktiverar immunsystemet på flera sätt. I likhet med ATOR-1015 aktiverar den det adaptiva immunförsvaret via CTLA-4. Detta är en väl validerad mekanism som ju nyligen tilldelades Nobelpris. Utöver detta aktiveras både det adaptiva och det ospecifika, ibland kallat det medfödda, immunförsvaret via målmolekylen GITR.
– Produkten lämpar sig särskilt väl för behandling av patienter med blodcancer, men förväntas också ha effekt mot solida tumörer. Dagens CTLA-4-läkemedel begränsas av svåra biverkningar, men ATOR-1144 har i likhet med ATOR-1015 möjlighet att undgå detta problem genom att den söker sig till tumörområdet.
Om vi backar några steg, kan du kort redogöra för bakgrunden till att Alligator Bioscience grundades år 2001?
– Alligator bildades ursprungligen för att kunna erbjuda andra företag proteinoptimering med hjälp av vår evolutionsteknologi FIND (Fragment-induced Diversity), men ganska snart inleddes utveckling av egna läkemedelskandidater. Alligator fokuserade så tidigt som 2008 helt på immunonkologi, d.v.s. flera år innan området var allmänt erkänt.
2015 tog du över rodret för bolaget. Vilka erfarenheter har du i bagaget som är extra viktiga i din nuvarande roll?
– Jag har 25 års erfarenhet av forskning inom farmakologi, läkemedelsvetenskap. Under de första 10 åren var detta ren grundforskning, men övergick därefter i klinisk läkemedelsutveckling. Som läkare specialiserade jag mig också mot läkemedelsutveckling, och efter specialistexamen i klinisk farmakologi gick jag vidare till läkemedelsindustrin. De senaste 12 åren har varit dedikerade till att leda och bygga organisationer för klinisk utveckling och utvärdering av nya läkemedelskandidater.
»James Allisons och Tasuku Honjos forskning har resulterat i ett helt nytt sätt att behandla cancer […] Våra bispecifika läkemedelskandidater ATOR-1015 och ATOR-1144, vilka kan ses som nästa generationens CTLA-4 antikroppar, är sprungna ur Allisons banbrytande upptäckter. ATOR-1015 är på väg att inleda klinisk utvecklingsfas, och vi är först i världen med ett nytt koncept, en bispecifik CTLA-4-antikropp som söker sig till tumörområdet«
Årets nobelpris i fysiologi eller medicin sätter globalt fokus på den spännande potentialen att utveckla nya behandlingsmetoder med hjälp av immunterapi. Vilken betydelse har pristagarna James P. Allisons och Tasuku Honjos upptäckter haft för detta område, och hur relaterar de till er FoU?
– James Allisons och Tasuku Honjos forskning har resulterat i ett helt nytt sätt att behandla cancer och Alligator har byggt vidare på de immunterapi-behandlingar som en gång etablerades av Allison och Honjo. I synnerhet våra bispecifika läkemedelskandidater ATOR-1015 och ATOR-1144, vilka kan ses som nästa generationens CTLA-4 antikroppar, är sprungna ur Allisons banbrytande upptäckter. ATOR-1015 är på väg att inleda klinisk utvecklingsfas, och vi är först i världen med ett nytt koncept, en bispecifik CTLA-4-antikropp som söker sig till tumörområdet.
På samma tema så tilldelades årets nobelpris i kemi Frances H Arnold, George P Smith och Sir Gregory P Winter för deras arbeten kring proteinevolution och fagdisplay. Det får nog anses vara helt unikt att två Nobelpris går att koppla till ett och samma bolag under samma år. Kan du berätta mer om beröringspunkterna mellan pristagarnas och ert arbete?
– Alligators grundare, professor Carl Borrebaeck, var med sin forskargrupp en av de första i fältet kring antikroppsdesign och arbetade tillsammans med Winter på 80-talet. Professor Borrebaeck ligger bakom flera av de rön som lade grunden för framgångarna inom utvecklingen av antikroppsbaserade läkemedel. En av teknologierna, FIND, som bland annat användes för att utveckla Alligators första läkemedelskandidat i klinik, är en förbättrad variant av den evolutionsteknologi som Arnold nu får Nobelpriset för.
»Janssen blev imponerade över det omfattande vetenskapliga datapaket som fanns vid handen, och den genomgående höga kvalitet som genomsyrade alla moment i utvecklingen. Avgörande var också att vi hade en god konkurrensposition, dvs att vår produkt låg i den absoluta framkanten i fältet«
För tre år sedan slog nyheten att ni hade slutit avtal med Janssen Biotech Inc., som ingår i den globala Johnson & Johnson-koncernen, tillika världens största hälsobolag, ned som en bomb. Avtalet är värt 6 miljarder kronor om cancerläkemedlet ADC-1013 går hela vägen till marknad. Vad imponerade mest på Janssen med detta utvecklingsprogram?
– Janssen blev imponerade över det omfattande vetenskapliga datapaket som fanns vid handen, och den genomgående höga kvalitet som genomsyrade alla moment i utvecklingen. Avgörande var också att vi hade en god konkurrensposition, dvs att vår produkt låg i den absoluta framkanten i fältet, och så förstås det faktum att vi hade optimerat ADC-1013 för ökad aktivitet i tumörmiljön, och kunde uppvisa övertygande data på att vår produkt hade potential för både kraftfull effekt och god tolerabilitet.
»Janssen beslutade i år inleda kombinationsstudier med ADC-1013 och deras PD-1-hämmare, vilket gav oss 6 miljoner USD i delmålsersättning«
Syftet med läkemedelskandidaten ADC-1013 är att stimulera immunsystemets dendritiska celler varpå T-cellerna skall bli mer aktiva mot tumören. Vad har hänt sedan avtalet undertecknades?
– Vi har framgångsrikt avslutat en klinisk fas I-studie och data presenterades i november 2017. Studien visade att ADC-1013 tolererades väl av cancerpatienter i kliniskt relevanta dosnivåer. Studien visade även att relevanta signalvägar för CD40 aktiverades av behandlingen vilket är en väldigt positiv signal. En patient förblev stabil i sin sjukdom i minst 12 mån och givet att det är svårt sjuka cancerpatienter i studien är det mycket intressant, även om det såklart får betraktas som anekdotiska data. Janssen beslutade i år inleda kombinationsstudier med ADC-1013 och deras PD-1-hämmare, vilket gav oss 6 miljoner USD i delmålsersättning.
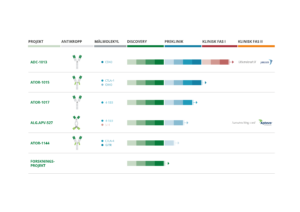
I juli 2017 ingick ni ett avtal med det amerikanska bioteknikbolaget Aptevo Therapeutics Inc. för gemensam utveckling av den bispecifika läkemedelskandidaten ALG.APV-527, vars effekt lokaliseras till tumörområdet och aktiverar de tumörspecifika immunceller som finns där. Vilka cancerformer har denna kandidat potential att behandla?
– ALG.APV-527 binder till både 5T4 och den co-stimulerande receptorn 4-1BB (CD137) och ska på så sätt ge en kraftfull och tumörriktad immunaktivering. 5T4 är ett tumörantigen som finns på en rad olika elakartade tumörtyper såsom icke-småcellig lung-, njur-, bukspottkörtel-, prostata- bröst-, kolorektal-, magsäcks-, äggstocks- och livmoderhalscancer. Däremot förekommer det knappt alls i normal vävnad vilket gör det till ett attraktivt mål för tumörriktad immunterapi av cancer.
I helgen presenterade Alligator och Aptevo Therapeutics positiva preklinisk data för ALG.APV-527 på Society for Immunotherapy of Cancer (SITC) 33rd Annual Meeting. Läs mer.
»En ansökan om att starta klinisk prövning d.v.s. studera en ny läkemedelskandidat i människa är ett stort steg. Det föregås av sammanställning av ett omfattande datapaket kring allt från tidiga resultat från laboratoriet till detaljer hur läkemedlet ska produceras i stor skala. Att ha detta avklarat är en avgörande milstolpe«
Två viktiga nyheter under årets tre första kvartal var att det prekliniska programmet för ATOR-1015 fullföljts och att ansökan om klinisk prövning har lämnats in, samt att ni har kunnat presentera nya prekliniska data som stödjer goda säkerhetsegenskaper för 4-1BB-antikroppen ATOR-1017. Kan du utveckla betydelsen av dessa nyheter?
– En ansökan om att starta klinisk prövning d.v.s. studera en ny läkemedelskandidat i människa är ett stort steg. Det föregås av sammanställning av ett omfattande datapaket kring allt från tidiga resultat från laboratoriet till detaljer hur läkemedlet ska produceras i stor skala. Att ha detta avklarat är en avgörande milstolpe. Vi är först i världen med ATOR-1015 och steget in i människa är såklart väldigt spännande. I ATOR-1015 har vi tagit konceptet med CTLA-4 som målmolekyl ett steg längre och ser med tillförsikt fram emot den fortsatta utvecklingen.
– ATOR-1017 är riktad mot målmolekylen 4-1BB och där ser vi nu en stor potential för ATOR-1017 att med sina tumörlokaliserande egenskaper ge både bättre effekt och förhoppningsvis betydligt färre biverkningar än konkurrenterna.
TeGeneros immunterarpi CD28-SuperMAB avvecklades år 2006 efter en katastrofal klinisk studie då flera försökspersoner drabbats av multiorgansvikt. Exemplet visar på svårigheterna att utveckla läkemedel som stimulerar immunförsvaret. Vad har hänt utvecklingsmässigt sedan dess och vilka lärdomar drog branschen av det inträffade?
– TeGeneros antikropp var en så kallad superagonistisk immunaktiverare som lyckades koppla bort immunsystemets säkerhetsmekanismer. Istället för att selektivt aktivera de immunceller som reagerar på kroppsfrämmande ämnen, som t.ex. vissa tumörstrukturer, aktiverades immunsystemet urskillningslöst. De immunonkologiska antikroppar som vi och andra bolag utvecklar idag aktiverar immunsystemet genom att dra nytta av naturliga förstärkande signalvägar, och risken för reaktioner av den svårighetsgrad som sågs för TeGeneros antikropp kan på så sätt minskas. Dock finns det naturligtvis kvarstående risker med läkemedel som aktiverar immunsystemet, och all utveckling av sådana produkter är väldigt väl kontrollerad.
»Alligator har valt att differentiera sig gentemot övriga bolag med hjälp av tumör-riktade läkemedelskandidater, d.v.s. produkter som söker sig till tumörområdet och är mer aktiva där än i övriga delar av kroppen. Målet är att ge färre biverkningar och ökad effekt«
Det var först med läkemedlet Yervoy (ipilimumab) år 2011 som immunterapi av metastaserad solid cancer blev en etablerad behandling. Hur ser konkurrenssituationen ut med immunterapi inom era valda indikationer?
– Givet att det är ett område med enorm marknadspotential är det såklart många aktörer som vill vara med och få en del av kakan. Alligator har valt att differentiera sig gentemot övriga bolag med hjälp av tumör-riktade läkemedelskandidater, d.v.s. produkter som söker sig till tumörområdet och är mer aktiva där än i övriga delar av kroppen. Målet är att ge färre biverkningar och ökad effekt.
Slutligen, vilka är de främsta anledningarna enligt dig till att cancersjukdomar fortfarande är en så svår utmaning för forskningen att knäcka, och vilken roll tror du att immunonkologi – som år 2013 utsågs till “Breakthrough of the Year” i tidskriften Science och i år alltså tilldelades Nobelpriset – kommer att spela i ett framtida behandlingsparadigm?
– Cancer är en komplex sjukdom där tumörcellerna har haft lång tid på sig att utveckla olika försvarsmekanismer. Därför kan cancern ofta anpassa sig till behandlingar som slår mot enskilda mekanismer, vilket leder till att effekten snabbt avtar. Immunterapi, som aktiverar kroppens eget immunförsvar mot cancern, leder till ett brett angrepp mot flera delar av cancercellerna, vilket gör det svårare för tumören att komma undan. Dessutom har immunsystemet förmågan att anpassa sig till förändringar i tumörcellerna och skapa ett immunologiskt minne mot tumören vilket möjliggör att cancern faktiskt kan botas.
– Det finns en stark drivkraft att utveckla nya, säkrare och mer effektiva immunterapier och kombinationsbehandlingar. Slutsatsen är att immunonkologi kommer att vara en integrerad del av nästan all cancerbehandling framöver, och att vi kommer att få se säkrare och mer effektiva immunterapier. I förlängningen gör detta att immunterapi kommer att kunna användas även vid mindre aggressiva cancer-varianter och tidigare i förloppet, vilket kommer att öka genomslaget ytterligare.
Per Norlén presenterar Alligator Bioscience vid BioStock Life Science Summit den 25 oktober 2018:

Mer om immunonkologi
Immunsystemet är kroppens skydd mot angrepp av sjukdomsalstrande mikroorganismer (som virus och bakterier) och av cancerceller. I växande tumörer finns ofta ett stort antal immunceller som har en inneboende förmåga att angripa cancercellerna. Men cancern utvecklar ofta ett eget skydd mot immunsystemet, bland annat genom att bilda immunhämmande ämnen.
Med immunterapi kan kroppens förmåga att bekämpa cancer förstärkas på ett effektivt sätt, vilket medför att tumörens försvar blockeras eller försvagas. De immunceller som oskadliggör cancercellerna kan sedan överleva i kroppen och utgör således ett skydd mot metastaser som eventuellt uppkommer efter avslutad behandling. Denna ”vaccinationseffekt” är unik för immunterapi.
Innehållet i Biostocks nyheter och analyser är oberoende men Biostocks verksamhet är i viss mån finansierad av bolag i branschen. Detta inlägg avser ett bolag som BioStock erhållit finansiering från. [et_bloom_inline optin_id=”optin_4″]

