NeuroVive når viktig milstolpe inom TBI i USA
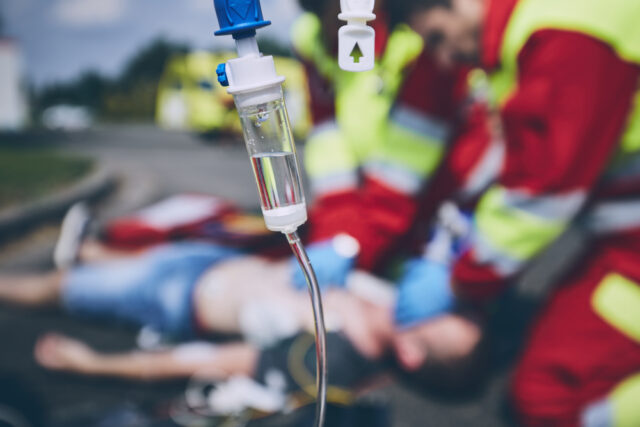
Årligen drabbas närmare 70 miljoner människor av traumatiska hjärnskador efter bland annat trafikolyckor och fallolyckor, likväl saknas idag effektiva behandlingar. Svenska NeuroVive har dock sett signaler om klinisk effekt med sin läkemedelskandidat NeuroSTAT och nu har bolagets IND-ansökan också godkänts av FDA, vilket öppnar upp för kliniska studier i USA.
Traumatiska hjärnskador (Traumatic Brain Injury, TBI) uppkommer vid externt våld mot huvudet med omedelbar skada på nervcellerna som följd. Dessa skador fortsätter sedan att förvärras under flera dagar efter det akuta traumat.
Enligt den amerikanska myndigheten Centers for Disease Control and Prevention, National Center for Injury Prevention and Control, så står TBI för hela 30 procent av alla skaderelaterade dödsfall i USA.
En tyst epidemi
TBI, som vanligen uppstår vid trafikolyckor, fallolyckor och vid misshandel, beräknas belasta den globala ekonomin med närmare 400 miljarder dollar årligen i direkta och indirekta vårdkostnader.
TBI kan påverka den kognitiva funktionen som t.ex. minnet och kan även leda till sämre motorik, hörsel, syn, nedsatt perception och beteende- och personlighetsförändringar som depression, ångest och aggression. Svår TBI kan leda till döden, eller resultera i koma, medan måttlig till svår TBI kan resultera i en förkortad livslängd.
Detta gör att TBI kan påverka alla aspekter av en persons liv, såsom familj- och vänskapsrelationer, men också förmågan att läsa vidare i skolan eller fortsätta arbeta, köra bil etc. Ett stort antal patienter kräver dessutom intensivvård och olika former av livslångt stöd.
»Vi är verkligen glada över den godkända IND-ansökan, som också är NeuroVives första. Det är en mycket viktig milstolpe och ett stort erkännande för projektet, och det är även värdefullt i våra diskussioner med möjliga externa samarbetspartners angående icke-utspädande finansiering och för fortsatt utveckling av NeuroSTAT«, säger NeuroVives vd Erik Kinnman i ett pressmeddelande
Målet med NeuroSTAT
NeuroVives kandidat mot traumatiska hjärnskador utvecklas i syfte att motverka uppkomsten av neurologiska och funktionella skador efter en traumatisk hjärnskada. Med en ny behandling som leder till ökad överlevnad, bättre livskvalitet och bevarad hjärnfunktion, hoppas NeuroVive att NeuroSTAT ska hjälpa de cirka 69 miljoner människor som drabbas årligen.
Särläkemedelsstatus i både Europa och USA
NeuroSTATs säkerhet, tolerabilitet och farmakokinetiska profil har tidigare utvärderats i en klinisk fas II-studie i Köpenhamn, CHIC-studien. Patientprover har också analyserats för biomarkörer vid hjärncellskada vilket gav en första signal om klinisk effekt. Läs en intervju här med Magnus Hansson, CMO på NeuroVive, om de genomförda biomarköranalyserna (okt 2018).
NeuroSTAT har dessutom särläkemedelsklassificering (Orphan Drug Designation) i både Europa och USA.
IND-ansökan godkänd av FDA
Idag stod det alltså klart att NeuroVives IND-ansökan (Investigational New Drug) har godkänts av den amerikanska läkemedelsmyndigheten, FDA. Den godkända ansökan är bolagets första och en fjäder i hatten för utvecklingen av NeuroSTAT.
En godkänd IND-ansökan krävs för att få använda läkemedel, som ännu inte finns på marknaden, i kliniska studier i USA. Ansökan måste innehålla detaljerad information om farmakologiska och toxikologiska studier, tillverkningsinformation, protokoll över föreslagna kliniska studier och information om de kliniska prövarnas kvalifikationer för att se till att studiedeltagarna inte utsätts för onödiga risker.
I september 2018 fick NeuroVive ett positivt utlåtande från FDA om sin utvecklingsplan för NeuroSTAT mot TBI. BioStock kommer, efter att NeuroVive nu har säkrat det viktiga tillståndet för läkemedelsprövning i USA, noga följa projektets kommande utvecklingssteg.
Läs även: Forskningsnätverk utlyser anslag för fas II-studie i TBI – lockar NeuroVive (15 jan 2019)
Innehållet i Biostocks nyheter och analyser är oberoende men Biostocks verksamhet är i viss mån finansierad av bolag i branschen. Detta inlägg avser ett bolag som BioStock erhållit finansiering från. [et_bloom_inline optin_id=”optin_4″]



