
LIDDS skapar möjligheter till effektiv och säker lokal cancerbehandling
Dagens läkemedelsbaserade cancerbehandlingar som ges i form av tabletter, sprutor eller infusion gör att stora delar av kroppen utsätts för läkemedlens effekter och biverkningar, inte bara själva tumören. Detta leder till onödigt svåra biverkningar vilket begränsar doseringen och påverkar patienternas livskvalitet negativt. LIDDS patenterade drug delivery-teknologi, NanoZolid, som kan kombineras med ett flertal olika läkemedelsmolekyler, ger en effektiv och kontrollerad lokal läkemedelseffekt, mindre biverkningar och färre doseringstillfällen vid lokalbehandling av cancertumörer. För att kunna fullfölja sina pågående kliniska studier och ta bolagets nya projekt till klinisk fas, genomför LIDDS just nu en kapitalanskaffning om totalt cirka 59,3 Mkr fördelad på en företrädesemission om cirka 37,1 Mkr och en riktad emission om cirka 22,3 Mkr.
 NanoZolid-teknologin gör det möjligt att injicera cancerläkemedel direkt i tumören. Förenklat kan man säga att LIDDS blandar in det aktiva läkemedlet i en patentskyddad suspension som injiceras i tumörområdet och bildar en solid depå från vilket läkemedlet utsöndras successivt i en förutbestämd och kontrollerad takt med effekt upp till sex månader.
NanoZolid-teknologin gör det möjligt att injicera cancerläkemedel direkt i tumören. Förenklat kan man säga att LIDDS blandar in det aktiva läkemedlet i en patentskyddad suspension som injiceras i tumörområdet och bildar en solid depå från vilket läkemedlet utsöndras successivt i en förutbestämd och kontrollerad takt med effekt upp till sex månader.
Nya läkemedelsprodukter efter robusta kliniska data
I maj kunde LIDDS publicera slutgiltiga data från en klinisk fas IIb-studie i bolagets längst framskridna projekt, Liproca Depot för behandling av prostatacancerpatienter under ”aktiv övervakning”. De positiva resultaten visade att Liproca Depot är en säker och effektiv behandling och studien mötte både primära och sekundära effektmått. MR-data visade att ingen av patienterna uppvisade någon progression av sjukdomen och några patienter uppvisade till och med en regression av tumören. Studieresultaten validerade NanoZolids potential och målet är nu att, baserat på dessa data, skapa nya läkemedelsprodukter riktat mot flera olika tumörsjukdomar.
Med NanoZolid har LIDDS framgångsrikt utvecklat en ny läkemedelskandidat med docetaxel. Docetaxel är ett vanligt läkemedel vid cytostatikabehandling av bröst-, prostata-, huvud- och hals-, mag- samt lungcancer. En placebokontrollerad preklinisk studie på NanoZolid i kombination med docetaxel visar tydliga effekter vid lokalbehandling av tumörer med lungcancerceller utan de svåra biverkningar som systemisk behandling ger. Forskningsresultaten har publicerats i den väl ansedda vetenskapliga tidskriften European Journal of Pharmaceutics and Biopharmaceutics. NanoZolid med docetaxel utvärderas just nu i en klinisk fas I-studie.

LIDDS står redo för nya avstamp och har under det senaste året utökat sin forskning inom bland annat immunonkologi och inlett flera forskningsprojekt som skall utvärdera hur NanoZolid-teknologin kan tillämpas för intratumoral immunterapi, d.v.s. där läkemedel injiceras direkt i cancertumören istället för intravenöst.
LIDDS har genomfört prekliniska studier med en specifik TLR9 agonist med positiva resultat och ett större prekliniskt program pågår som kommer att slutföras under 2020. TLR9-aktivering i tumörer kan leda till att immunsystemet aktiveras mot tumören genom att celldödande T-celler stimuleras. T-cellsaktivering är ett nödvändigt steg för att skapa en tumörbekämpande effekt.
Målsättningen är att en fas I-studie ska inledas under 2021, där NanoZolid-TLR9-produkten kan komma att kombineras med en checkpoint-hämmare. NZ-TLR9 har i djurmodeller visat på minskad tumörtillväxt och ökad överlevnad. Resultaten hittills bekräftar att NanoZolid i kombination med TLR9 ger en depåeffekt som är nödvändig eftersom TLR9 är en mycket kortverkande molekyl som bara kan behandla ytliga tumörer som annars begränsar den kommersiella potentialen. NanoZolid i kombination med en STING-agonist är ytterligare ett immunterapiprojekt där möjlighet till utlicensiering finns efter att det prekliniska programmet slutförts.
Utlicensiering är kärnan i affärsmodellen
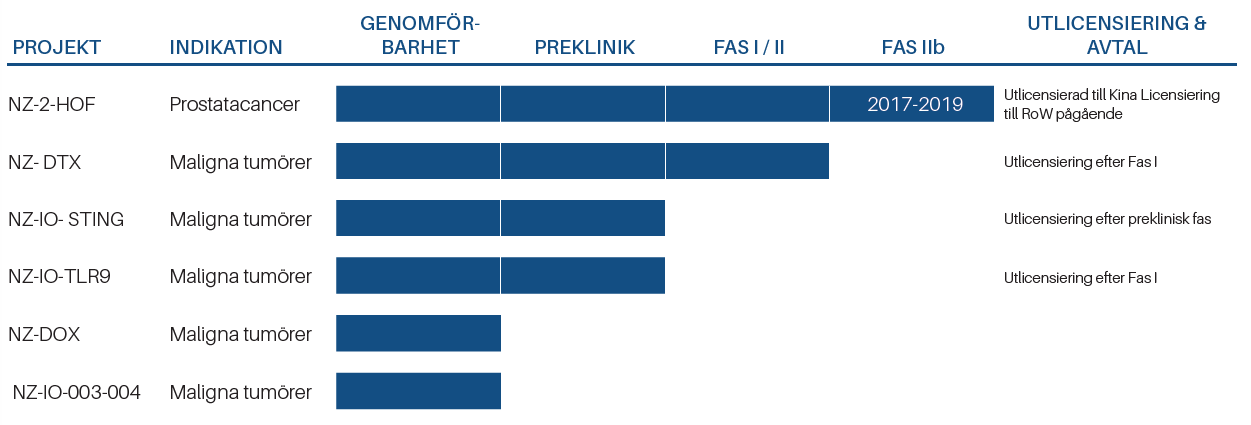
LIDDS mål är att utlicensiera sina egenutvecklade projekt efter preklinisk fas, eller efter att initiala kliniska studier har genomförts. Bolaget är även öppet för att licensiera ut själva NanoZolid-teknologin till andra läkemedelsbolag för användning i deras egna utvecklingsprocesser.
Genom att utlicensiera efter preklinik, alternativt efter fas I/II-data, menar bolaget att de egna investeringarna kan minimeras och möjliggöra ett positivt kassaflöde betydligt snabbare än om bolaget på egen hand skulle driva projekten hela vägen till marknad.
Ytterligare en fördel, givet att bolagets projekt baseras på redan beprövade läkemedelssubstanser, är att utvecklingsrisken är begränsad samtidigt som utvecklingstiden är avsevärt kortare jämfört med utveckling av ett helt nytt läkemedel.
LIDDS licenstagare kan förbättra sina produkter och skjuta fram patentstupet
Bolagets patent för NanoZolid ger ett IP-skydd till år 2037 för läkemedelskandidater som baseras på plattformen. Detta medför goda möjligheter till förlängning av produktlivscykeln för redan etablerade läkemedelssubstanser som är på väg att förlora, eller redan har förlorat, sitt patentskydd. I praktiken innebär detta att tillverkare av originalläkemedel ges en möjlighet att förbättra sina produkter och få en ökad livslängd genom att licensiera LIDDS patenterade teknologi.
NanoZolid-plattformen – som har erhållit 132 nationella patent som täcker samtliga stora marknader – ger även LIDDS möjligheter att bredda sin egen projektportfölj. Olika läkemedelssubstanser kan integreras i den patentskyddade plattformsteknologin och därmed skapa nya läkemedelsprodukter för användning vid en rad olika tumörsjukdomar.
LIDDS har framgångsrikt re-formulerat ett antal olika typer av läkemedel. Ett exempel på detta är 2-hydroxyflutamide, ett vanligt cancerläkemedel som idag används för behandling av prostatacancer och som är den aktiva substansen i Liproca Depot.
Mot fas III-studier
I november 2019 inleddes förberedelserna inför en större fas III-studie i prostatacancer med Liproca Depot i samband med att bolagets kinesiska partner, Jiangxi Puheng Pharma, inledde diskussioner med det kinesiska läkemedelsmyndigheten. I april 2020 mottog LIDDS även positiva svar från svenska Läkemedelsverket som inte föreslog några förändringar av bolagets design av fas III-studien.
Läkemedelsverket bekräftade även att en enda pivotal fas III-studie med positiva studieresultat kan vara tillräcklig för ett framtida marknadsgodkännande för Liproca Depot.
Kapitalinjektion om 59,3 Mkr
I syfte att tillföra bolaget rörelsekapital för att kunna fullfölja pågående kliniska studier, samt ta nya projekt till klinisk fas, genomför LIDDS just nu en kapitalanskaffning om totalt cirka 59,3 Mkr.
Denna är fördelad på en företrädesemission om cirka 37,1 Mkr och en redan genomförd riktad emission med avvikelse från aktieägarnas företrädesrätt om cirka 22,3 Mkr. Likviden avses täcka bolagets kapitalbehov för den kommande tolvmånadersperioden.
Nettolikviden avses användas till följande områden:
- Cirka 40 procent till NZ-TLR9-projektet där NanoZolid kombineras med en TLR9-agonist
- Cirka 25 procent till att driva NZ-IO-projektet – där NanoZolid kombineras med immunonkologiska kandidater i forskning och utvecklingsfas – till att initiera en fas I-studie
- Cirka 35 procent till pågående projekt och allmänna företagsändamål
[divider]ERBJUDANDET I SAMMANDRAG[/divider]
EMISSIONSBELOPP |
37,1 Mkr före avdrag för transaktionskostnader. |
TECKNINGSKURS |
12 SEK per aktie. Courtage utgår ej. |
FÖRETRÄDESRÄTT & TECKNINSRÄTT |
En (1) befintlig aktie berättigar till en (1) teckningsrätt och åtta (8) teckningsrätter ger rätt att teckna en (1) ny aktie.
|
TECKNINGSPERIOD |
23 juni – 7 juli
|
HANDEL MED TECKNINGSRÄTTER |
23 juni – 3 juli 2020 |
HANDEL MED BTA |
23 juni till omkring 16 juli |
TECKNINGSFÖRBINDELSER & GARANTIÅTAGANDEN |
Bolagets styrelseledamöter och flera ledande befattningshavare har åtagit sig att teckna sina respektive pro rata-andelar av Företrädesemissionen. Dessa teckningsförbindelser uppgår till totalt cirka 3,1 Mkr, motsvarande cirka 8,2 procent av Företrädesemissionen. Vissa av Bolagets större aktieägare har åtagit sig att teckna sina respektive pro rata-andelar av Företrädesemissionen. Dessa teckningsförbindelser uppgår till totalt cirka 2,8 Mkr motsvarande cirka 7,5 procent av Företrädesemissionen. Därutöver har Bolaget erhållit garantiåtaganden om cirka 31,3 Mkr motsvarande cirka 84,3 procent av Företrädesemissionen. Företrädesemissionen omfattas således till 100 procent av teckningsförbindelser och garantiåtaganden. Emissionsgarantierna är inte säkerställda. |
UTSPÄDNING |
Den Riktade Emissionen innebär en utspädning för befintliga aktieägare om cirka 7,0 procent av antalet aktier och röster i bolaget. |
OFFENTLIGGÖRANDE AV UTFALL |
9 juli |
[divider]DOKUMENT & INFO[/divider]


Artikelns innehåll är sponsrat av det aktuella bolaget som förekommer i texten. BioStock tillhandahåller inte investeringsrådgivning, förmedlar inga investeringsorder och tar inget ansvar för agerande och/eller eventuell förlust eller skada av något slag som grundar sig på användandet av innehåll som publicerats på BioStock.se. Varje investeringsbeslut fattas istället självständigt av den enskilde investeraren.



