
Brexit – Läkemedelsindustrin stålsätter sig inför EMA:s flytt till Amsterdam
Brexit-omröstningen skakade om Europa och efterskalven är påtagliga inom läkemedelsindustrin. Så snart Brexit (till synes) var ett faktum tog EU beslutet att flytta EMA från London, ett drag som redan har haft betydande inverkan på sektorn. BioStock har kikat närmare på hur flytten av myndigheten till Amsterdam har, och kommer att, påverka life sciencebranchen när nu stafettpinnen har bytt händer.
Den europeiska läkemedelsmyndigheten EMA (European Medicines Agency) är ett av de största regulatoriska organen inom EU och en av de första att påverkas av Brexit. Efter folkomröstningen i juni 2016 fattade EU:s tillsynsmyndighet beslutet att flytta EMA huvudkontor från London. I november 2017 stod det klart att Amsterdam gått vinnande ur striden med Milano om att bli myndighetens nya hemvist.
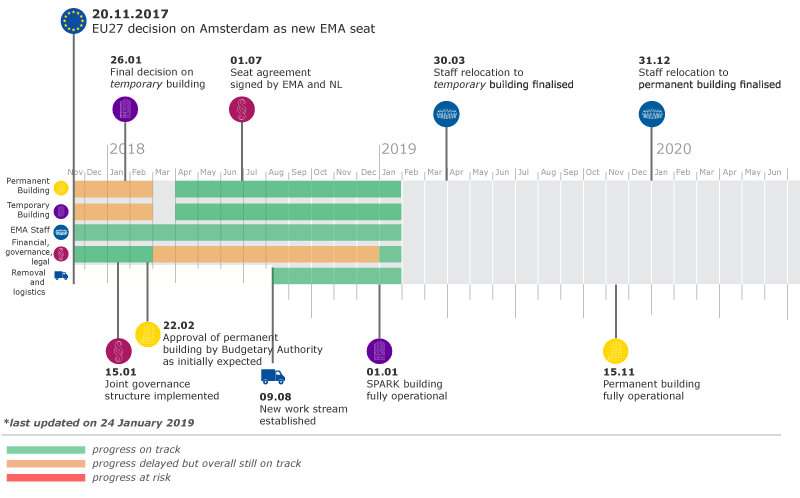
Den fysiska flytten inleddes i början av denna månad, med målet att de flesta av myndighetens 900 anställda skulle arbeta vid Amsterdam-kontoret innan Brexit verkställdes, vilket till nyligen var planerat att ske idag den 29 mars 2019.
Den nederländska regeringen har underlättat flytten genom att tillhandahålla läkemedelsmyndigheten en tillfällig byggnad tills det permanenta huvudkontoret byggts färdigt. Den slutliga flytten planeras vara klar innan årets slut.
EMA: s roll
EMA har i uppgift att främja utvecklingen av, och tillgången till, läkemedel. Myndigheten reglerar tillstånd för de läkemedel som marknadsförs i EU – både för människor och djur – och spelar därmed en avgörande roll för life science-sektorns bioteknik-, läkemedels- och medicinbolag. Mer specifikt tillhandahåller EMA bolagen med riktlinjer för vad som anses vara tillräckligt för att påvisa att ett läkemedel är säkert och effektivt. EMA utvärderar sedan läkemedelkandidatens kliniska evidens och fattar beslut om huruvida den är säker för slutkonsumenten, alltså patienten. Man följer även upp dessa parametrar efter produktlansering.
EMA är förberett på förseningar
Den massiva flytten och en stram tidsfrist på 16 månader har satt myndighetens möjligheter att uppfylla sina skyldigheter på spel, inte minst då vissa resurser har fått omallokeras från regulatoriska till logistiska aktiviteter. Utmaningarna förstärks av det faktum att inte alla London-anställda kommer att följa med till Amsterdam, utan EMA förväntar sig att förlora 25 procent av sin personalstyrka i flytten.
EMA har emellertid sjösatt en välarbetad kontinuitetsplan för att förhindra alltför stora driftsstörningar gällande godkännande, underhåll och övervakning av läkemedel under flyttprocessen. Vidare inrättades Brexit-relaterade riktlinjer för att motverka förseningar rörande läkemedelsdistribution och marknadsgodkännanden.
Regulatoriska utmaningar för läkemedelsbolag
Trots ansträngningarna från EMA får branschen sannolikt räkna med utdragna ledtider och läkemedelsbolagen stålsätter sig nu inför en potentiell “hård”, eller avtalslös, Brexit. Oavsett vilken uppgörelse mellan EU och Storbritannien som till slut blir verklighet, så beklagar experter bristen på tydliga besked kring huruvida den regulatoriska processen kommer skilja sig åt mellan de två slutliga regionerna, och i så fall hur mycket. Väntan på en slutlig dom i frågan har sannolikt en betydande inverkan på läkemedelsbolagens planeringsstrategier.
En av de mest troliga konsekvenserna av en hård Brexit för det regulatoriska landskapet är obligatorisk certifiering av produkter i både EU och Storbritannien. Det skulle medföra studier, eller åtminstone omformulerade beslutsunderlag, för respektive region. Något som också skulle resultera i högre kostnader för tillverkarna. Ett sådant scenario skulle kunna undvikas genom ett potentiellt Brexit-avtal.
Brexit verkställdes uppenbarligen inte idag då Storbritannien lyckats förlänga sin Brexit-deadline till 12 april, då det återigen är dags att stålsätta sig för ett potentiellt besked om en “no-deal” Brexit. Ett sådant scenario, där parterna inte lyckas enas om ett avtal, skulle skapa en ännu högre grad av osäkerhet för såväl life science-bolag som för marknaden i stort.
»Manufacturers with strong regulatory resources, intelligence and structure will be much better prepared to navigate the changing regulation landscapes, and these well-prepared companies will, no doubt, position themselves as the most competitive in the market.« – Paul Brooks, Executive Director vid Regulatory Affairs Professionals Society (RAPS)
Londons förlust innebar samtidigt en vinst för Amsterdam
Tiden kommer utvisa slutnotan för Brexit och EMA-flytten. Men vad som redan nu kan konstateras är att det som blev en stor förlust för London och Storbritannien, nu istället kommer att gynna Amsterdam. Det gäller inte bara 900 arbetstillfällen utan också utsikten för framtida life science-investeringar. För att strö salt i britternas och staden Londons sår, har även den amerikanska läkemedelsmyndigheten FDA beslutat att följa med EMA till Amsterdam och flytta sitt Europakontor dit. För Amsterdam betyder EMA-flytten istället att man får se staden växa till en av Europas mest relevanta huvudstäder.
Innehållet i Biostocks nyheter och analyser är oberoende men Biostocks verksamhet är i viss mån finansierad av bolag i branschen. Detta inlägg avser ett bolag som BioStock erhållit finansiering från. [et_bloom_inline optin_id=”optin_4″]



