Immunovia lockar storspelare till världens största pankreasstudie
Immunovia utvecklar blodtestet IMMray PanCan-d för tidig diagnos av pankreascancer, en sjukdom där upp till 85 procent av de diagnostiserade har för långt framskriden sjukdom för att kunna behandlas. En lång rad namnkunniga amerikanska och europeiska universitet och sjukhus har redan anslutit sig till Immunovias kliniska multicenterstudie för tidig upptäckt av pankreascancer. Målet är att validera testet i patienter med ärftlig risk för pankreascancer, s.k familjär pankreascancer. Enligt en nyligen publicerad artikel i Journal of Clinical Oncology, visar Immunovias test i stora forskningsstudier en träffsäkerhet på 96-98 procent för pankreascancer.
Tidig upptäckt förbättrar 5-årsöverlevnaden 10 gånger
På grund av att det är svårare att nå lyckosamma behandlingsutfall i de senare sjukdomsstadierna, indikerar tidigare diagnoser att betydligt fler skulle kunna räddas än nya behandlingsmetoder. Serumprover från blod kan enligt Immunovia öka chanserna för tidigare upptäckter och därigenom förbättra patienternas 5-årsöverlevnad till 50 procent, från dagens 5-8 procent. Mot denna bakgrund har bolaget utvecklat IMMray PanCan-d för tidig diagnos av pankreascancer.
Valideringen av testet väcker globalt intresse hos renommerade institutioner
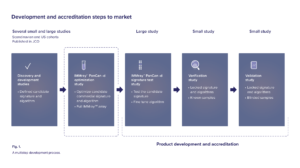
För nästan exakt två år sedan inleddes den första kliniska valideringsstudien för IMMray PanCan-d. PanFAM-1 undersöker testets kapacitet till tidig upptäckt av pankreascancer bland personer med ärftlig risk för pankreascancer. Sedan dess har en lång rad högt respekterade internationella sjukhus och universitet anslutit sig till studien. Förra månaden tillkom ytterligare fyra: McGill, Yale och universitetssjukhusen i både Pennsylvania och Massachusetts. Läs om övriga deltagare här.
2000 individer skall testas i USA och Europa
Med målet att validera Immunovias blodtest, IMMray PanCan-d, ska studien analysera blodprover från mer än tvåtusen individer i Sverige, USA och Europa över en treårsperiod. De inkluderade patienterna har redan erbjudits FPC-screeningsprogram för familjär eller ärftlig pankreascancer.
Syftet med valideringen av IMMray PanCan-d är att dokumentera ett förbättrat utfall för cancerpatienterna och att påvisa de övergripande hälsovårdsfördelarna med att testa personer med ärftlig risk för pankreascancer i en prospektiv studie. I förlängningen är detta ett krav för att den amerikanske läkemedelsmyndigheten FDA ska godkänna testet samt för att det ska kvalificera sig för kostnadsersättning i olika försäkringssystem.
Parallellt med PanFAM-1 genomför Immunovia två ytterligare valideringsstudier. Den ena, PanSYM-1, inkluderar patienter med vaga symptom på pankreascancer medan den andra, PanDIA-1, riktar in sig på en annan identifierad högriskgrupp, nämligen nyligen diagnostiserade diabetiker över 50 år, som löper en större risk för pankreascancer de första 3 åren efter typ 2 diabetesdiagnosen.
Nuvarande metoder har begränsningar
IMMray-plattformen mäter immunförsvarets sjukdomsrespons genom ett mönster av proteiner i blodet som är specifika för olika sjukdomar, en respons som uppstår omedelbart när tumören bildas.
Idag används generellt vävnadsbiopsi som ett diagnostiskt verktyg för att konstatera pankreascancer. Men vävnadsbiopsier svarar enbart på om det finns en tumör på den testade platsen i kroppen och utfallet är beroende av att man lyckas biopsera den rätta delen av tumören. Eftersom olika tumörställen kan ha olika genotyper och fenotyper kan vävnadsbiopsier därför ge missvisande svar. Dessutom har olika delar av tumören ofta genetiskt distinkta grupper av celler, inte minst i pankreascancer.
Konkurrerande blodtester
Det finns för närvarande inga tillförlitliga blodtest för att diagnostisera pankreascancer på marknaden. Dock används två olika blodtester i dagsläget i klinisk vardag – ett test för höga halter av hormoner som kan tillämpas för att identifiera sällsynta former av pankreascancer, såsom insulinom och gastrinom, samt ett test för förhöjda nivåer av bilirubin och leverenzym som kan användas för att undersöka om cancern blockerar gallgången.
Därtill används idag två blodtester för att övervaka om en patient svarar på behandlingen, men de kan inte användas för diagnostiska ändamål eftersom inte alla patienter med pankreascancer får förhöjda nivåer av de aktuella biomarkörerna. Dessutom kan vissa andra hälsotillstånd som inte är cancer ge utslag på dessa biomarkörer. Därför används dessa tester enbart för att övervaka behandling, inte för diagnostiska ändamål.
Diagnosen pankreascancer fastställs idag med hjälp av magnetkameraundersökning (MR och MRCP) och/eller med en endoskopisk ultraljudsundersökning.
Behovet av ett enkelt test som tidigt kan diagnostisera pankreascancer, samt följa upp behandlingsrespons med hög precision, är därmed stort. Immunovia hoppas att IMMray PanCan-d ska kunna möta efterfrågan på tidig detektion av pankreascancer. Interimsresultat från de stora kliniska valideringsstudierna PanFAM-1, PanSYM-1 och PanDIA-1, som skulle kunna understödja denna förhoppning, väntas i slutet av nästa år och slutresultatet 2020/2021. Immunovias test, IMMray PanCan-d beräknas nå marknaden i slutet av 2019 i USA och början av 2020 som CE-märkt test i Europa.
Om pankreascancer
Pankreascancer är en av de mest dödliga och svårupptäckta cancertyperna då tecken och symptom är diffusa och liknar de hos andra sjukdomar. I enbart USA dör över 40 000 och fler än 50 000 nya fall diagnostiseras årligen och överlevnaden på fem års sikt är för närvarande 5-8 procent. Prognosen säger att cancertypen kommer att vara den näst dödligaste år 2020. Eftersom resektion är mer framgångsrikt i stadium I/II kan dock tidig diagnos avsevärt förbättra cancerpatienters överlevnad på fem års sikt potentiellt från 5-8 procent upp till 49 procent.
Se vd Mats Grahn presentera bolaget vid Vator Securities Unicorn Summit 10 oktober 2018:
Innehållet i Biostocks nyheter och analyser är oberoende men Biostocks verksamhet är i viss mån finansierad av bolag i branschen. Detta inlägg avser ett bolag som BioStock erhållit finansiering från.