
Analysuppdatering: NeuroVive Pharmaceutical
NeuroVive Pharmaceutical hade ett tufft år på börsen 2015 och bolagsvärdet minskade kraftigt efter två rapporterade bakslag under året. Dels föll den prövarinitierade fas III-studien med NeuroVives läkemedelskandidat CicloMulsion inom indikationen reperfusionsskada i samband med PCI för STEMI hjärtpatienter på grund av utebliven effekt. Vidare meddelade licenstagaren av NeuroVives läkemedelskandidat NVP-018, Arbutus Biopharma, att man avbrutit vidareutvecklingen av substansen för kronisk hepatit B. Men i skuggan av dessa två negativa besked har NeuroVive under innevarande år i ett högt tempo fortsatt att utveckla sin portfölj i såväl kliniska som prekliniska program. Även forskningsportföljen har under året tagit kliv framåt. Dessa utvecklingsframsteg gör nu att NeuroVive under hösten 2016 har en rad mycket viktiga milstolpar att rapportera från flera olika projekt i portföljen.
Analysen löper över två sidor.
Efter NeuroVives tuffa 2015 har bolagsvärdet fallit kraftigt till dagens historiskt låga nivåer. Men samtidigt som aktiemarknaden har värderat ner bolagets framgångschanser har bolaget fortsatt att utveckla sina tillgångar, förstärkt organisationen och ledningen och ändrat inriktningen, från marknadslansering och kommersialisering, till FoU och uppbyggnad av nya värden i portföljen.
Bolaget har idag två pågående kliniska projekt, båda i fas II, som kommer att färdigrekryteras och visa resultat under andra halvåret 2016. Utöver det är bolagets läkemedelskandidat NVP019 i slutfasen av sitt prekliniska program och kan, om allt går bra, gå in i människa 2017. Samtidigt pågår hög aktivitet i NeuroVives delägda brittiska forskningsbolag Isomerase Therapeutics där såväl NVP014 som utvecklas för Stroke och NVP015 för energireglering kan nå nya milstolpar under innevarande år. Bolaget har också informerat om att det finns flera forskningsprogram som utvecklas hos Isomerase inom nya områden och nya indikationer, som kommer att presenteras i samband med att patentansökningarna för dessa program publiceras.
Med tanke på det digra program av betydande milstolpar som NeuroVive har framför sig i närtid så finns det goda möjligheter för bolaget att återigen få se sitt bolagsvärde öka och för bolagets ägare att återigen kunna se på framtiden med tillförsikt.
NeuroVive genomför just nu en företrädesemission för att kunna genomföra de högt ställda utvecklingsplanerna och nå de milstolpar som krävs för att bygga upp värdet på nytt i bolagets portfölj.
NeuroVive – Ledande inom mitokondriell medicin
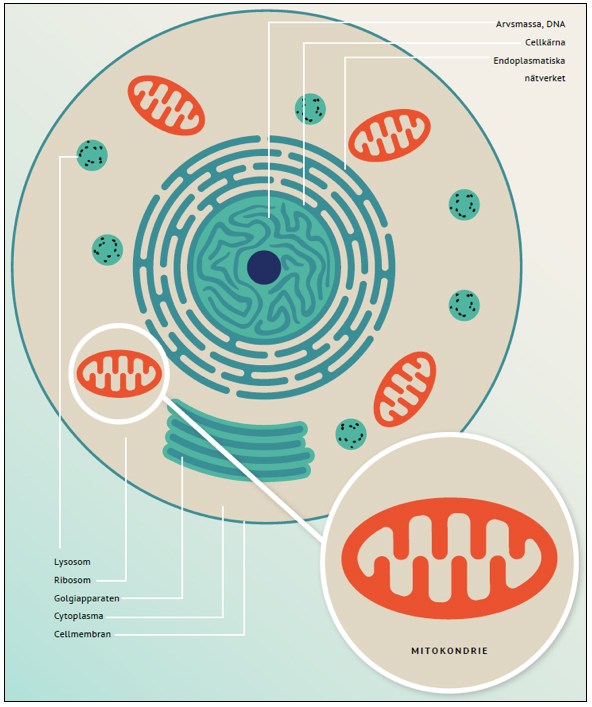
NeuroVive anses vara bland de ledande bolagen i världen inom forskning och utveckling av mitokondriell medicin. Ett område som många utanför medicinvetenskapen kanske inte har så stora kunskap om. Mitokondrier finns i nästan alla celler och är cellens motor som förser cellen med energi. Om mitokondrierna inte fungerar så får inte cellen nödvändig energi och dör. Förenklat så omvandlar mitokondrierna den näring i form av mat och dryck som vi sätter i oss till energi för cellen. Mitokondrierna är alltså helt avgörande för att cellerna och därmed också organen i kroppen ska fungera och att vi alla ska kunna kliva upp ur sängen varje morgon.
Mitokondriell medicin omfattar alla sjukdomstillstånd, såväl akuta som kroniska, där mitokondriernas funktion är nedsatt och därmed påverkar cellernas funktion negativt. Sådana akuta tillstånd har t.ex. föreslagits vara skallskada (TBI), upphört blodflöde till hjärnan (Stroke), rubbat blodflöde till njurarna i samband med stor kirurgi och vid andra akuta trauman där närliggande celler dör eller skadas då mitokondrierna funktion är kraftigt försvagad. Forskning och studier har visat att defekter på mitokondrierna kan ligga till grund för en rad olika sjukdomstillstånd. Utöver akuta trauman samt akuta eller kroniska hjärnskador så är även all typ av organsvikt och diabetes exempel på tillstånd som kan ha stor nytta av mediciner som kan stödja den mitokondriella funktionen.
NeuroVives primära fokus inom mitokondriell medicin är för akuta tillstånd. Bolaget utvecklar så kallade cyklofilinhämmare som effektivt skyddar mitokondriernas funktion och därmed potentiellt kan kraftigt begränsa den primära skadeutvecklingen vid t.ex. stor kirurgi, traumatisk hjärnskada, stroke och akut organsvikt. Det finns också ett stort antal genetiska sjukdomar som direkt drabbar mitokondriernas funktion för vilka NeuroVive utvecklar helt nya kemiska läkemedelssubstanser som förväntas öka mitokondriernas energiutveckling, de så kallade energireglerarna (NVP015).
Läkemedelskandidater i klinisk utvecklingsfas.
CicloMulsion
CicloMulsion utvecklas för organskydd vid akuta sjukdomsförlopp. Den aktiva substansen Cyklosporin-A i CicloMulsion har funnit på marknaden i över 30 år och har använts av miljontals patienter som genomgått organtransplantation i syfte att minska avstötningen av nya organ. NeuroVives grundare och forskningschef Eskil Elmér upptäckte för mer än 20 år sedan att Cyklosporin-A också är starkt cellskyddande. Flera av varandra oberoende akademiska forskargrupper runt om i världen har genom åren gjort olika försök och tester som bekräftar den ursprungliga upptäckten, och som styrker NeuroVives tes om att deras läkemedelskandidater CicloMulsion & NeuroSTAT kan skydda och rädda celler t.ex. i samband med reperfusion.
Förra året rapporterade CIRCUS-studien resultat. Studien, som var prövarinitierad, leddes professor Michael Ovize vid universitetssjukhuset i Lyon (HCL) och var till stor del finansierad av HCL genom en rad olika franska och europeiska anslag. Studien, en fas III-studie, undersökte effekten av CicloMulsion för patienter drabbade av hjärtinfarkt som genomgick akut PCI-operation (PPCI), vilket är en operation som genomförs när patienten har en pågående hjärtinfarkt. CicloMulsion skulle i denna patientgrupp ges ca 10 minuter innan den akuta operationen och därmed skydda hjärtcellerna för skada som uppkommer när blodflödet normaliseras i hjärtat efter genomförd PPCI-operation. Resultatet i studien var nedslående för NeuroVive då man för denna indikation, reperfusionsskada i samband med PCI för s.k. STEMI hjärtpatienter, inte kunde se något positivt resultat av att använda CicloMulsion istället för placebo.
Varför resultatet uteblev är inte helt kartlagt ännu, men enligt NeuroVive och forskarna knutna till den externa studien kan en huvudorsak ha varit att CicloMulsion helt enkelt inte kom fram i tid till cellerna och mitokondrierna i infarktsområdet, dvs den del av hjärtat som behövde skyddas.
Reperfusionsskada anses ske mycket snabbt efter återställt blodflöde, troligtvis så snabbt att det är svårt för något läkemedel som getts i blodbanan att hinna utöva sin effekt före att skadan är etablerad. Den problematiken har sannolikt varit gemensam för samtliga läkemedelskandidater som genom åren har testats kliniskt för denna indikation. Reperfusionsskadan sker när blodflödet åter släpps på och när syrgas åter tränger in i cellerna. Alla molekyler likt cyklosporin, som är en större molekyl än syrgas, tränger in i vävnaden lite långsammare från blodbana genom hjärtmuskelcellerna till mitokondrierna.
Även om studien i sig var ett misslyckande så tillfördes CicloMulsion säkerhetsdata från knappt 500 behandlade patienter. Inga allvarliga incidenter som kan härledas till användandet av CicloMulsion rapporterades från studien. Detta är naturligtvis positivt i skenet av att omkring 25 procent av alla kandidater som inte når marknad och som befinner sig i fas II-studier faller just p.g.a. dålig säkerhet och biverkningar.

CicloMulsion testas nu för njurskydd för patienter som genomgår hjärtkirurgi, kranskärlsoperationer
Njurskyddsstudien heter CiPRICS (Ciclosporin to Protect Renal function In Cardiac Surgery) och är en dubbelblind, randomiserad och placebokontrollerad klinisk fas II-studie som inkluderar totalt 150 patienter. Patienterna kommer att behandlas med CicloMulsion i samband med kranskärlsoperationer på Thoraxkliniken vid Skånes universitetssjukhus i Lund. Även denna studie är prövarinitierad och drivs av Skånes universitetssjukhus med visst stöd från NeuroVive.
När patienterna ska genomgå denna kirurgi, som är ett planerat och inte akut ingrepp, så kopplas hjärtat ur och ersätts av en hjärt- och lungmaskin. Detta kan skapa skador på framförallt njurarna som utsätts för en enorm stress när blodflödet och därmed syresättning till cellerna i njuren rubbas. Många patienter som genomgår denna typ av kirurgi drabbas därför av sämre njurfunktion och i vissa fall av livslång njursvikt och dialysbehandling.
Det finns några viktiga skillnader med denna studie jämfört med CIRCUS-studien som inte visade resultat. I CIRCUS studien skulle CicloMulsion skydda från utökad skada. Den initiala skadan på hjärtat var redan orsakad i och med hjärtinfarkten. I CiPRICS-studien sätts CicloMulsion in innan skadeförloppet börjar. Dessutom kan CicloMulsion ges mer kontrollerat och ges tid att fullt ut nå fram och in i cellerna innan man startar operationen. Detta är möjligt eftersom det rör sig om en planerad operation och inte en akut situation, som i fallet med en patient som har en pågående hjärtinfarkt.
NeuroVive har även flaggat för att man planerar att följa upp denna studie med en mindre dosstudie i denna patientgrupp för att undersöka om andra dosnivåer kan ge andra effekt- och säkerhetsdata. Beroende på resultatet i studien kan bolaget också välja att stoppa utvecklingen av CicloMulsion och istället inrikta utvecklingen helt på bolagets uppföljare NVP-019.
NeuroVive har kommunicerat att njurstudien kommer att vara färdigrekryterad och rapportera resultat under andra halvåret 2016.
Denna studie kan möjligen vara CicloMulsion sista chans i kliniska utvecklingsprogram. Resultatet blir helt avgörande för om CicloMulsion har en framtida möjlighet att nå marknadsgodkännande för denna eller någon annan indikation.
Patentskyddet för CicloMulsion är inte optimalt utan består av formuleringspatent som visserligen är förnyade och långa men som inte erbjuder samma skydd som ett patent på grundsubstansen kan ge. Detta begränsar naturligtvis möjligheterna till riktigt stora licensaffärer med CicloMulsion.
Marknads- & Värdekalkyl CicloMulsion
Vid hjärtkirurgi stoppas i regel hjärtat under själva operationen och ersätts då av en hjärt-lungmaskin för att syresätta och pumpa runt blodet till kroppens alla olika delar. Det innebär en mycket stor påfrestning för kroppens mest energikrävande organ som t.ex. njurarna.
Behandlingen med CicloMulsion inför operation kan bli aktuell för alla patienter som genomgår hjärtkirurgi med hjärt-lungmaskin. Enbart i USA genomförs omkring 700 000 sådana operationer årligen. Tillsammans med marknaden i Europa och även vissa marknader i Asien bedömer vi att marknaden omfattar 1,5 miljoner patienter årligen.
Med en genomsnittlig behandlingskostnad med CicloMulsion om 10 000 SEK så är den teoretiska marknadspotentialen 15 miljarder SEK per år.
Det finns idag inga läkemedel på marknaden som kan skydda njurarna eller andra organ från att skadas för dessa patienter. Vi har räknat med en genomsnittlig marknadspenetration om 15 procent samt att CicloMulsion licensieras ut till en partner som genomför fas III-studie och regulatoriskt arbete för marknadsgodkännande. I ett sådant affärsförhållande har vi kalkylerat med att NeuroVive för Europa och USA-marknaden får i genomsnitt 15 procent i royalty. I Kina har NeuroVive redan en partner i Sihuan Pharmaceutical som ger 10 procent i royalty på framtida försäljning av CicloMulsion, oavsett indikation.
NeuroVive har även ett sedan länge pågående skiljedomsförfarande med Ciclomulsion AG, varifrån NeuroVive för längesedan licensierade in emulsionen CicloMulsion. Ett avgörande utslag kommer i närtid och skall avgöra om NeuroVive fortsättningsvis är bundna av att betala royalty på eventuella framtida intäkter på CicloMulsion. Vi har i vår värdekalkyl räknat med att NeuroVive ska betala 10 procent royalty på sina intäkter från läkemedelskandidaten.
NeuroSTAT
NeuroSTAT är namnet på NeuroVives läkemedelskandidat för hjärn- och nervskador. NeuroSTAT är identiskt med CicloMulsion men preparatet har helt enligt praxis givits olika namn beroende på indikation, applikationsområde och behandlingsform.
Traumatisk hjärnskada (TBI) är en skada på hjärnan som uppkommer efter externt våld mot huvudet där nervcellerna tar omedelbar skada och där skadorna förvärras i flera dagar, ibland veckor, efter tillbudet vilket utvecklar en väsentligt större total skada.

NeuroSTAT utvärderas just nu i en fas IIa-studie som genomförs på Rigshospitalet i Köpenhamn
Den pågående CHIC-studien i Köpenhamn är en mycket viktig studie. Den är i första hand en dos- och säkerhetsstudie där man undersöker säkerheten för patienterna i två olika dosnivåer. Varje dos nivå omfattar 10 patienter och den första lägre dosnivån är färdigrekryterad – man har nu rekryterat 5 av 10 patienter i den högre dosnivån.
Utöver dos- och säkerhet så undersöks också en rad andra parametrar, däribland i hur hög grad läkemedlet faktiskt når fram och kan verka i det skadade området i hjärnan.
Studien är en s.k. open-label studie och inte placebokontrollerad. Efter att den första dos-nivån var färdigrekryterad genomfördes en noggrann säkerhetskontroll av en oberoende säkerhetskommitté som gav sitt godkännande att påbörja rekryteringen av patienter till den högre dos-nivån.
TBI är ett väldigt komplicerat terapiområde och det saknas idag läkemedel som kan begränsa skadeutvecklingen. Det är också en indikation med stora utmaningar rent regulatoriskt och kliniskt. Ett 30-tal studier har misslyckats genom åren och myndigheterna har därför idag börjat utarbeta nya praxis för studiedesign för att erhålla marknadsgodkännande. Den största utmaningen är att i placebokontrollerade effektstudier kunna jämföra utfallen mellan patientgrupperna. Varje hjärnskada kan sägas vara unik och därför svår att jämföra mot en placebogrupp.
Men förutsättningarna håller som sagt på att ritas om för att bedriva fas III-studier inom detta område och det blir avgörande för NeuroVive och partners att myndigheterna kan tillåta alternativa effektmätningar för att man ska kunna nå framgång regulatoriskt.
NeuroVive har kommunicerat att man förväntar sig att den högre dosgruppen blir färdigrekryterad i år och att resultat kan rapporteras sent 2016 eller under första kvartalet 2017.
Parallellt med det kliniska utvecklingsarbetet genomför NeuroVive tillsammans med Universitetet i Pennsylvania (PENN) prekliniska effektstudier med NeuroSTAT på stora djur i avancerade modeller. PENNs forskningskluster för TBI anses vara ledande i världen på prekliniska experimentella modeller för TBI. Även från dessa prekliniska studier kommer NeuroVive att rapportera resultat under 2016.
CicloMulsion ges med en dos vid ett tillfälle medan NeuroSTAT ges på ett annat sätt. Först ges en dos så nära inpå skadetillfället som möjligt. Därefter startas en kontinuerlig infusion som pågår i fem dagar. Den lägre dosen i studien är 5 mg/kg/dag och den högre dosen är 10 mg/kg/dag.
Den snart avslutade kliniska studien, tillsammans med de prekliniska resultaten, ska hjälpa NeuroVive i uppsättningen av kliniska effektstudier, fas IIb- och III-studier. Detta tillsammans med partners som kan vara såväl kommersiella som ideella. Såväl amerikanska som kinesiska militärorganisationer har visat intresse för att stödja den fortsatta utvecklingen av NeuroSTAT då deras personal ofta drabbas av TBI i sina uppdrag.
I Kina har NeuroVive redan en partner för fas III-studier i licenstagaren Sihuan Pharmaceutical.
Precis som för CicloMulsion så saknas för NeuroSTAT patent på grundsubstansen, och man har istället skyddat produkten med formuleringspatent som är förnyade och sträcker sig bortom 2030. För indikationen svår till medelsvår TBI har NeuroVive däremot beviljats särläkemedelsklassificering i både EU och USA vilket ger marknadsexklusivitet efter marknadsgodkännande i sju år i USA och i tio år inom EU. Uppnådd särläkemedelsstatus är i många fall ett starkare marknadsskydd än patent.
Marknads- & värdekalkyl NeuroSTAT
Svår TBI är mycket kostsamt för samhället. Den totala vårdkostnaden för en enda patient med svår TBI är uppskattningsvis mellan 5-15 miljoner kronor. De direkta vårdkostnaderna för svåra skallskador i enbart Europa och USA överstiger svindlande 70 miljarder kronor. Inkluderar man därtill de indirekta kostnaderna i form av sjukskrivningar och förlorade skatteintäkter från förvärvsarbete uppgår dessa i enbart USA, allt enligt de senaste uppskattningarna till över 700 miljarder kronor. Behovet av ett läkemedel som i positiv riktning kan påverka dessa siffror är stort.
Antalet fall av TBI uppgår årligen i världen till omkring 10 miljoner. De fall som är av svårare art och som NeuroSTAT kan komma att användas till uppgår till 1,2 miljoner patienter per år varav 450 000 av dessa är på de viktiga marknaderna i USA och Europa.
Till skillnad från CicloMulsion, som enbart ges i en dos vid ett tillfälle, ges NeuroSTAT över en period av minst fem dagar vilket ger ett högre pris per behandlad patient. Det tillsammans med särläkemedelsstatusen och indikationens komplexitet och enorma behov gör att vi sätter behandlingskostnaden till 30 000 SEK per patient vilket ger en årlig total marknadspotential om 36 miljarder SEK.
Om man kommer först till marknad med NeuroSTAT för i första hand svår TBI så är det stor chans att man snabbt når väldigt hög marknadspenetration då behandlingsalternativen totalt sett är få för patienterna, samtidigt som samhällskostnaderna är betydande.
Vi räknar dock med en marknadspenetrering om ett snitt av 15 procent över den kalkylerade försäljningsperioden, där USA, Europa och vissa regioner och länder i Asien kommer att stå för en betydande del av den totala marknaden för NeuroVive och NeuroVives partners.
Vi har i vår kalkylmodell också räknat med att NeuroSTAT licensieras ut till en partner som genomför fas III-studie och regulatoriskt arbete för marknadsgodkännande. I ett sådant affärsförhållande har vi kalkylerat med att NeuroVive för Europa och USA-marknaderna får i genomsnitt 15 procent i royalty och på de asiatiska marknaderna i snitt 10 procent i royalty. I Kina har NeuroVive redan en partner i Sihuan Pharmaceutical som ger 10 procent i royalty på framtida försäljning av NeuroSTAT, oavsett indikation.
OBS: analysen fortsätter på sida 2.



